Kimia / Kelas X / Ikatan Kimia
Selain gas mulia, unsur-unsur pada tabel periodik berada di alam dalam bentuk senyawa (dua unsur atau lebih yang berikatan). Hal ini menunjukkan bahwa unsur-unsur tersebut tidak stabil untuk berdiri sendiri. Ketidakstabilan ini berhubungan dengan konfigurasi elektron tersebut.
Lewis dan Langmuir menyatakan bahwa gas mulia sulit untuk berikatan dengan unsur lain karena elektron valensinya sudah penuh. Konfigurasi elektron gas mulia tertera seperti pada tabel ini:
Melihat hal ini, kita bisa menyimpulkan bahwa suatu atom yang memiliki konfigurasi elektron seperti gas mulia akan stabil, dengan kata lain unsur-unsur tersebut membentuk senyawa agar konfigurasinya mengikuti gas mulia. Suatu atom dapat mencapai konfigurasi elektron gas mulia dengan melepaskan elektron valensi, menangkap elektron, ataupun memakai elektronnya untuk 2 atom secara bersamaan.
Lewis dan Langmuir menyatakan bahwa gas mulia sulit untuk berikatan dengan unsur lain karena elektron valensinya sudah penuh. Konfigurasi elektron gas mulia tertera seperti pada tabel ini:
| Unsur | Konfigurasi |
| Helium | 2 |
| Neon | 2 8 |
| Argon | 2 8 8 |
| Krypton | 2 8 18 8 |
| Xenon | 2 8 18 18 8 |
| Radon | 2 8 18 32 18 8 |
Senyawa yang terbentuk dari satu unsur melepaskan elektronnya dan unsur lain menangkapnya adalah senyawa ion. Ikatan yang terbentuk dari 2 unsur ini disebut ikatan ion. Serah-terima elektron ini menyebabkan satu unsur bermuatan positif dan satunya bermuatan negatif. Akibat muatan yang berlawanan ini terjadi gaya tarik-menarik yang membentuk ikatan ion. Atom yang bermuatan positif karena melepaskan elektron disebut dengan kation, atom yang menerima elektron dan bermuatan negatif disebut anion.
Atom natrium melepaskan 1 elektron membentuk kation Na+ yang konfigurasinya sama seperti neon: 2 8.
Pada saat yang bersamaan, klorin menangkap elektron ini membentuk Cl- yang memiliki konfigurasi seperti argon 2 8 8.
Sehingga persamaan reaksi ini sepenuhnya menjadi NaCl yang merupakan ikatan ionik:
Pada pembentukan kation, jumlah elektron yang dilepas sama dengan nomor golongan. Untuk anion, jumlah elektron yang diterima sama dengan delapan dikurangi nomor golongannya.
Atom natrium melepaskan 1 elektron membentuk kation Na+ yang konfigurasinya sama seperti neon: 2 8.
Na ➝ Na+ + e-
Cl + e- ➝ Cl-
Na+ + Cl- ➝ NaCl
Menurut Lewis, unsur-unsur non logam dapat membentuk ikatan dengan atom non logam lainnya melalui penggunaan bersama elektron valensinya. Mengapa atom non-logam ini tidak melakukan serah terima elektron seperti ikatan ion?
Atom-atom non logam umumnya berada pada golongan VA-VIIA memiliki elektron valensi yang terbilang banyak sehingga sulit untuk melepaskan elektronnya. Untuk mencapai konfigurasi stabil seperti gas mulia, atom-atom tersebut cenderung menge-share elektronnya untuk dipakai bersama. Ikatan yang terbentuk dari sharing elektron ini disebut dengan ikatan kovalen. Senyawa yang terbentuk disebut dengan senyawa kovalen. Berikut adalah jenis-jenis ikatan kovalen:
Ikatan kovalen tunggal
Seperti namanya, ikatan kovalen tunggal adalah ikatan yang terbentuk dari 2 atom yang masing-masing menyumbangkan 1 elektronnya untuk dipakai bersama sebagai sepasang elektron. Contoh ikatan ini adalah asam klorida HCl. H di sini memiliki 1 elektron dan disumbangkan untuk dipakai bersama. Cl memiliki 7 elektron dan salah satunya disumbangkan untuk dipakai bersama. Sepasang elektron yang dishare bisa dilambangkan dengan garis.
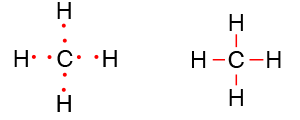
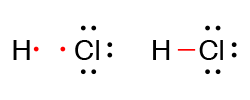 Contoh lainnya adalah metana CH4 di mana H memiliki 1 elektron dan C memiliki 4 elektron. Semua elektron ini dishare untuk dipakai bersama.
Contoh lainnya adalah metana CH4 di mana H memiliki 1 elektron dan C memiliki 4 elektron. Semua elektron ini dishare untuk dipakai bersama.
Ikatan kovalen rangkap
Selain ikatan kovalen tunggal ada juga ikatan kovalen rangkap 2 atau 3. Ikatan kovalen rangkap terjadi jika jumlah elektron yang dishare oleh masing-masing atom yang berikatan berjumlah 2 atau 3. Contohnya pada O2, 1 atom O memiliki konfigurasi elektron 2 6. Untuk mencapai konfigurasi gas mulia yang terdekat Ne dengan konfigurasi elektron 2 8, atom oksigen ini membutuhkan 2 elektron lagi. Untuk memecahkan masalah ini masing-masing atom O men-sharing 2 elektronnya sehingga terjadi ikatan rangkap.
 Contoh lainnya adalah N2, di mana N memiliki konfigurasi elektron 2 5. Untuk mencapai konfigurasi gas mulia diperlukan 3 elektron lagi, maka masing-masing atom N menyumbang 3 elektron sehingga terjadi ikatan rangkap 3.
Contoh lainnya adalah N2, di mana N memiliki konfigurasi elektron 2 5. Untuk mencapai konfigurasi gas mulia diperlukan 3 elektron lagi, maka masing-masing atom N menyumbang 3 elektron sehingga terjadi ikatan rangkap 3.
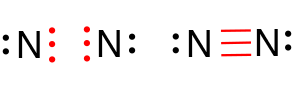
Ikatan kovalen polar
Molekul diatom seperti H2, O2, dan N2 memiliki daya tarik menarik antara dua atom yang sama besar karena keduanya memiliki keelektronegatifan yang sama. Apa yang terjadi ketika 2 molekul yang memiliki keelektronegatifan yang berbeda seperti pada asam klorida HCl? Cl memiliki keelektronegatifan 3,1 dan H 2,1. Maka Cl memiliki daya tarik terhadap elektron yang lebih besar daripada H. Akibatnya pasangan elektron ini akan lebih dekat ke arah atom klorin.
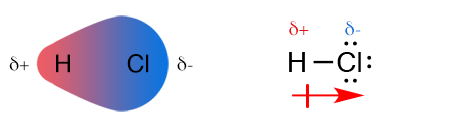 Hal ini menyebabkan pengkutuban muatan. Oleh karena elektron lebih medekat ke klorin maka klorin membentuk kutub negatif, di lain sisi hidrogen membentuk kutub positif. Molekul HCl sendiri itu bersifat netral maka besarnya muatan negatif di klorin harus sama dengan muatan positif pada hidrogen. Kutub positif dan negatif dalam senyawa kovalen ini juga merupakan pemisahan muatan secara parsial bukan keseluruhan seperti pada ikatan ion. Pengkutuban muatan ini dilambangkan dengan δ.
Hal ini menyebabkan pengkutuban muatan. Oleh karena elektron lebih medekat ke klorin maka klorin membentuk kutub negatif, di lain sisi hidrogen membentuk kutub positif. Molekul HCl sendiri itu bersifat netral maka besarnya muatan negatif di klorin harus sama dengan muatan positif pada hidrogen. Kutub positif dan negatif dalam senyawa kovalen ini juga merupakan pemisahan muatan secara parsial bukan keseluruhan seperti pada ikatan ion. Pengkutuban muatan ini dilambangkan dengan δ.
Pada senyawa kovalen yang memiliki pengkutuban muatan ini dinamakan dengan ikatan kovalen polar. Pemisahan muatan secara parsial ini terjadi akibat perbedaan keelektronegatifan dari atom-atom.
Ikatan kovalen koordinasi
Dalam ikatan kovalen kedua atom yang berikatan sama-sama menyumbangkan elektronnya. Mungkinkah ikatan kovalen terjadi jika hanya satu atom yang menyumbangkan elektronnya? Berdasarkan dari senyawa yang ditemukan, ternyata ada senyawa kovalen yang elektronnya hanya berasal dari satu atom. Ikatan kovalen yang seperti ini dinamakan dengan ikatan kovalen koordinasi.
Contoh ikatan ini adalah ion amonium NH4+. Ion ini terbentuk dari ikatan amonia NH3 dan ion hidrogen H+. NH3 sendiri adalah senyawa kovalen di mana hidrogen menyumbangkan 1 elektron dan nitrogen 3 elektron untuk berikatan. Setelah itu ada ion H+ yang tidak memiliki elektron, maka sisa 2 elektron di nitrogen yang belum dishare dipakai bersama dengan ion H+ membentuk ikatan kovalen koordinasi.
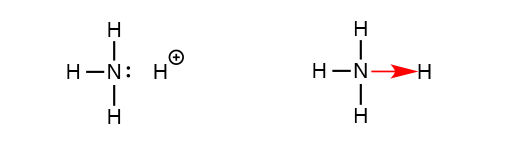 Jika ikatan kovalen dinyatakan dengan bentuk garis, ikatan kovalen koordinasi ini dinyatakan dengan bentuk anak panah. Anak panah ini ujungnya dari atom yang menyumbang elektron dan menuju ke atom yang menerima elektron tersebut.
Jika ikatan kovalen dinyatakan dengan bentuk garis, ikatan kovalen koordinasi ini dinyatakan dengan bentuk anak panah. Anak panah ini ujungnya dari atom yang menyumbang elektron dan menuju ke atom yang menerima elektron tersebut.
Atom-atom non logam umumnya berada pada golongan VA-VIIA memiliki elektron valensi yang terbilang banyak sehingga sulit untuk melepaskan elektronnya. Untuk mencapai konfigurasi stabil seperti gas mulia, atom-atom tersebut cenderung menge-share elektronnya untuk dipakai bersama. Ikatan yang terbentuk dari sharing elektron ini disebut dengan ikatan kovalen. Senyawa yang terbentuk disebut dengan senyawa kovalen. Berikut adalah jenis-jenis ikatan kovalen:
Ikatan kovalen tunggal
Seperti namanya, ikatan kovalen tunggal adalah ikatan yang terbentuk dari 2 atom yang masing-masing menyumbangkan 1 elektronnya untuk dipakai bersama sebagai sepasang elektron. Contoh ikatan ini adalah asam klorida HCl. H di sini memiliki 1 elektron dan disumbangkan untuk dipakai bersama. Cl memiliki 7 elektron dan salah satunya disumbangkan untuk dipakai bersama. Sepasang elektron yang dishare bisa dilambangkan dengan garis.
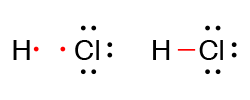

Ikatan kovalen rangkap
Selain ikatan kovalen tunggal ada juga ikatan kovalen rangkap 2 atau 3. Ikatan kovalen rangkap terjadi jika jumlah elektron yang dishare oleh masing-masing atom yang berikatan berjumlah 2 atau 3. Contohnya pada O2, 1 atom O memiliki konfigurasi elektron 2 6. Untuk mencapai konfigurasi gas mulia yang terdekat Ne dengan konfigurasi elektron 2 8, atom oksigen ini membutuhkan 2 elektron lagi. Untuk memecahkan masalah ini masing-masing atom O men-sharing 2 elektronnya sehingga terjadi ikatan rangkap.

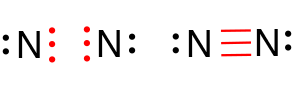
Ikatan kovalen polar
Molekul diatom seperti H2, O2, dan N2 memiliki daya tarik menarik antara dua atom yang sama besar karena keduanya memiliki keelektronegatifan yang sama. Apa yang terjadi ketika 2 molekul yang memiliki keelektronegatifan yang berbeda seperti pada asam klorida HCl? Cl memiliki keelektronegatifan 3,1 dan H 2,1. Maka Cl memiliki daya tarik terhadap elektron yang lebih besar daripada H. Akibatnya pasangan elektron ini akan lebih dekat ke arah atom klorin.

Pada senyawa kovalen yang memiliki pengkutuban muatan ini dinamakan dengan ikatan kovalen polar. Pemisahan muatan secara parsial ini terjadi akibat perbedaan keelektronegatifan dari atom-atom.
Ikatan kovalen koordinasi
Dalam ikatan kovalen kedua atom yang berikatan sama-sama menyumbangkan elektronnya. Mungkinkah ikatan kovalen terjadi jika hanya satu atom yang menyumbangkan elektronnya? Berdasarkan dari senyawa yang ditemukan, ternyata ada senyawa kovalen yang elektronnya hanya berasal dari satu atom. Ikatan kovalen yang seperti ini dinamakan dengan ikatan kovalen koordinasi.
Contoh ikatan ini adalah ion amonium NH4+. Ion ini terbentuk dari ikatan amonia NH3 dan ion hidrogen H+. NH3 sendiri adalah senyawa kovalen di mana hidrogen menyumbangkan 1 elektron dan nitrogen 3 elektron untuk berikatan. Setelah itu ada ion H+ yang tidak memiliki elektron, maka sisa 2 elektron di nitrogen yang belum dishare dipakai bersama dengan ion H+ membentuk ikatan kovalen koordinasi.
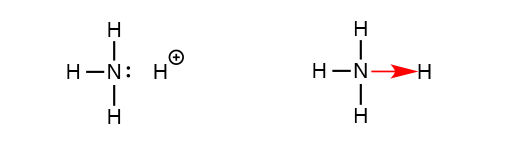
Logam dan bukan logam membentuk ikatan ion, sesama non logam membentuk ikatan kovalen. Ikatan apa yang terjadi ketika unsur logam bertemu dengan unsur logam? Logam dan logam ini membentuk yang disebut kristal logam dan mempunyai sifat-sifat fisik tertentu yaitu:
Teori lautan elektron
Teori ikatan logam pertama kali dikembangkan oleh Drude dan kemudian disempurnakan oleh Lorentz sehingga teori ini sering dikenal sebagai teori elektron bebas atau teori elektron dari Drude-Lorentz. Berdasarkan teori ini, kristal logam tersusun atas kation-kation logam yang tak bergerak dan dikelilingi oleh lautan elektron valensi yang bergerak bebas dalam sisi kristal. Ikatan logam terbentuk antara kation logam dan elektron valensi.
Elektron valensi logam bergerak bebas dan mengisi ruangan di antara kisi-kisi kation logam yang bermuatan positif. Oleh karena elektron ini bergerak bebas, maka elektron ini bisa berpindah jika dipengaruhi oleh medan listrik atau panas.
Sifat mengkilap logam
Menurut teori Drude-Lorentz, jika cahaya mengenai permukaan logam, sebagian dari elektron valensi logam akan tereksitasi ke kulit yang lebih tinggi. Saat elektron ini kembali kembali ke posisi awalnya atau tereksitasi ke kulit yang lebih rendah, energi dibebaskan dalam bentuk cahaya atau kilap. Peristiwa inilah yang membuat permukaan logam mengkilap.
Konduktor listrik dan panas
Listrik bisa mengalir pada logam karena adanya elektron valensi yang bergerak bebas dalam kristal logam. Jika listrik dialirkan melalui logam, elektron-elektron valensi logam akan membawa arus listrik ke seluruh logam dan bergerak menuju potensial yang lebih rendah sehingga terjadi aluran listrik dalam logam tersebut.
Hal ini terjadi juga dengan panas. Saat panas atau kalor diserap, elektron-elektron valensi logam akan bergerak lebih cepat dan membawa kalor yang diserap. Akibatnya, panas ini bisa didistribusikan ke seluruh kristal logam sehingga seluruh bagian logam menjadi panas.
Lentur
Lentur di sini yang dimaksud adalah mudah ditempa dan dibentuk tetapi tidak mudah patah. Hal ini juga berkaitan dengan lautan elektron. Saat logam ditempa atau dibentuk terjadi pergeseran kation-kation tetapi ini tidak menyebabkan patah karena setiap kation selalu dikelilingi oleh lautan elektron.
Jika kita bandingkan dengan NaCl yang memiliki ikatan ionik, saat ditempa akan terjadi pergeseran ion-ion, ion-ion yang baru ini bisa bersifat tolak menolak sehingga mengakibatkan patahnya kristal NaCl menjadi serbuk-serbuk.
Teori lautan elektron
Teori ikatan logam pertama kali dikembangkan oleh Drude dan kemudian disempurnakan oleh Lorentz sehingga teori ini sering dikenal sebagai teori elektron bebas atau teori elektron dari Drude-Lorentz. Berdasarkan teori ini, kristal logam tersusun atas kation-kation logam yang tak bergerak dan dikelilingi oleh lautan elektron valensi yang bergerak bebas dalam sisi kristal. Ikatan logam terbentuk antara kation logam dan elektron valensi.
Elektron valensi logam bergerak bebas dan mengisi ruangan di antara kisi-kisi kation logam yang bermuatan positif. Oleh karena elektron ini bergerak bebas, maka elektron ini bisa berpindah jika dipengaruhi oleh medan listrik atau panas.
Sifat mengkilap logam
Menurut teori Drude-Lorentz, jika cahaya mengenai permukaan logam, sebagian dari elektron valensi logam akan tereksitasi ke kulit yang lebih tinggi. Saat elektron ini kembali kembali ke posisi awalnya atau tereksitasi ke kulit yang lebih rendah, energi dibebaskan dalam bentuk cahaya atau kilap. Peristiwa inilah yang membuat permukaan logam mengkilap.
Konduktor listrik dan panas
Listrik bisa mengalir pada logam karena adanya elektron valensi yang bergerak bebas dalam kristal logam. Jika listrik dialirkan melalui logam, elektron-elektron valensi logam akan membawa arus listrik ke seluruh logam dan bergerak menuju potensial yang lebih rendah sehingga terjadi aluran listrik dalam logam tersebut.
Hal ini terjadi juga dengan panas. Saat panas atau kalor diserap, elektron-elektron valensi logam akan bergerak lebih cepat dan membawa kalor yang diserap. Akibatnya, panas ini bisa didistribusikan ke seluruh kristal logam sehingga seluruh bagian logam menjadi panas.
Lentur
Lentur di sini yang dimaksud adalah mudah ditempa dan dibentuk tetapi tidak mudah patah. Hal ini juga berkaitan dengan lautan elektron. Saat logam ditempa atau dibentuk terjadi pergeseran kation-kation tetapi ini tidak menyebabkan patah karena setiap kation selalu dikelilingi oleh lautan elektron.
Jika kita bandingkan dengan NaCl yang memiliki ikatan ionik, saat ditempa akan terjadi pergeseran ion-ion, ion-ion yang baru ini bisa bersifat tolak menolak sehingga mengakibatkan patahnya kristal NaCl menjadi serbuk-serbuk.
Senyawa ion dan kovalen berbeda dalam proses pembentukkannya, maka kedua senyawa ini juga memiliki sifat fisika dan kimia yang berbeda.
Kemudahan menguap
Coba kita bandingan antara cuka yang merupakan senyawa kovalen dan garam yang merupakan senyawa ion. Dari antara dua benda ini, kita akan mudah sekali mencium baunya cuka. Hal ini dikarenakan oleh cuka lebih mudah menguap atau memiliki titik didih yang relatif rendah daripada garam. Pada tekanan normal, cuka memiliki titik didih 119 oC sedangkan garam pada 1517 oC. Kemudahan menguap suatu zat dipengaruhi oleh gaya tarik antar molekul.
Gaya tarik antar molekul itu berbeda dengan gaya tarik antar atom. Gaya tarik antar atom adalah tarikan antara atom-atom yang membentuk suatu molekul atau senyawa (yang membuat ikatan kovalen atau ion). Sedangkan gaya tarik antar molekul adalah tarikan antara molekul-molekul dalam suatu senyawa yang berdampak pada wujud zat tersebut.
Pada senyawa kovalen, gaya tarik antar molekulnya cukup rendah sehingga pada umumnya senyawa kovalen lebih mudah menguap dibandingkan senyawa ion.
Daya hantar listrik
Logam dapat menghantarkan listrik karena adanya lautan elektron yang dapat bergerak bebas. Apakah senyawa ion dan kovalen dapat menghantarkan listrik?
Jika kita melakukan eksperimen dengan garam natrium klorida kita akan menemukan bahwa dalam wujud padat NaCl tidak dapat menghantarkan listrik tetapi jika dicairkan akan dapat menghantarkan listrik. Hal ini disebabkan karena pada keadaan padat, senyawa ion membentuk kisi-kisi kristal yang kaku. Kation dan anion nya berikatan dengan sangat kuat sehingga tidak dapat bergerak bebas. Karena tidak bisa bergerak, maka senyawa ini tidak bisa menghantarkan arus listrik. Ketika dicairkan atau dilelehkan, tarikan antara kation dan anion ini melemah sehingga dapat bergerak bebas. Hasilnya, saat arus listrik dilewatkan, ion-ion tersebut dapat menghantarkan arus listrik dari yang berpotensial tinggi ke yang lebih rendah.
Pada senyawa kovalen, baik dalam wujud padat ataupun cair tidak dapat menghantarkan arus listrik. Artinya, tidak terjadi pemisahan atom-atom membentuk ion yang bermuatan listrik, melainkan tetap sebagai molekul kovalen. Oleh karena tidak terbentuk ion yang bermuatan listrik, maka saat arus listrik dialirkan tidak ada ion yang bisa menghantarkan daya arus ini.
Kelarutan
Bagaimanakah kelarutan senyawa ion dan kovalen pada berbagai macam pelarut?
Jika kita melihat tiga senyawa: garam NaCl, naftalena, dan gula dan mencoba pada 3 macam jenis pelarut yaitu air, alkohol, dan benzena. Kita akan menemukan bahwa NaCl hanya larut dalam air. Naftalena hanya larut pada benzena. dan gula larut dalam air dan alkohol.
Berdasarkan fakta dari eksperimen ini, kita bisa melihat bahwa senyawa ion (contohnya NaCl di sini) larut dalam air tetapi tidak larut dalam pelarut organik. Pada umumnya, senyawa ion larut dalam air tetapi beberapa zat tertentu ternyata tidak larut.
Jika kita lihat senyawa kovalen: gula dan naftalena – sifat kelarutan mereka berbeda. Hal ini dikarenakan gula merupakan kovalen polar sedangkan naftalena adalah kovalen nonpolar. Air dan alkohol merupakan senyawa polar maka bisa melarutkan gula yang juga polar. Benzena adalah senyawa nonpolar sehingga bisa melarutkan naftalena yang nonpolar.
Pada umumnya, senyawa kovalen polar larut dalam pelarut polar, senyawa kovalen nonpolar larut dalam pelarut nonpolar.
Kemudahan menguap
Coba kita bandingan antara cuka yang merupakan senyawa kovalen dan garam yang merupakan senyawa ion. Dari antara dua benda ini, kita akan mudah sekali mencium baunya cuka. Hal ini dikarenakan oleh cuka lebih mudah menguap atau memiliki titik didih yang relatif rendah daripada garam. Pada tekanan normal, cuka memiliki titik didih 119 oC sedangkan garam pada 1517 oC. Kemudahan menguap suatu zat dipengaruhi oleh gaya tarik antar molekul.
Gaya tarik antar molekul itu berbeda dengan gaya tarik antar atom. Gaya tarik antar atom adalah tarikan antara atom-atom yang membentuk suatu molekul atau senyawa (yang membuat ikatan kovalen atau ion). Sedangkan gaya tarik antar molekul adalah tarikan antara molekul-molekul dalam suatu senyawa yang berdampak pada wujud zat tersebut.
Pada senyawa kovalen, gaya tarik antar molekulnya cukup rendah sehingga pada umumnya senyawa kovalen lebih mudah menguap dibandingkan senyawa ion.
Daya hantar listrik
Logam dapat menghantarkan listrik karena adanya lautan elektron yang dapat bergerak bebas. Apakah senyawa ion dan kovalen dapat menghantarkan listrik?
Jika kita melakukan eksperimen dengan garam natrium klorida kita akan menemukan bahwa dalam wujud padat NaCl tidak dapat menghantarkan listrik tetapi jika dicairkan akan dapat menghantarkan listrik. Hal ini disebabkan karena pada keadaan padat, senyawa ion membentuk kisi-kisi kristal yang kaku. Kation dan anion nya berikatan dengan sangat kuat sehingga tidak dapat bergerak bebas. Karena tidak bisa bergerak, maka senyawa ini tidak bisa menghantarkan arus listrik. Ketika dicairkan atau dilelehkan, tarikan antara kation dan anion ini melemah sehingga dapat bergerak bebas. Hasilnya, saat arus listrik dilewatkan, ion-ion tersebut dapat menghantarkan arus listrik dari yang berpotensial tinggi ke yang lebih rendah.
Pada senyawa kovalen, baik dalam wujud padat ataupun cair tidak dapat menghantarkan arus listrik. Artinya, tidak terjadi pemisahan atom-atom membentuk ion yang bermuatan listrik, melainkan tetap sebagai molekul kovalen. Oleh karena tidak terbentuk ion yang bermuatan listrik, maka saat arus listrik dialirkan tidak ada ion yang bisa menghantarkan daya arus ini.
Kelarutan
Bagaimanakah kelarutan senyawa ion dan kovalen pada berbagai macam pelarut?
Jika kita melihat tiga senyawa: garam NaCl, naftalena, dan gula dan mencoba pada 3 macam jenis pelarut yaitu air, alkohol, dan benzena. Kita akan menemukan bahwa NaCl hanya larut dalam air. Naftalena hanya larut pada benzena. dan gula larut dalam air dan alkohol.
| NaCl | Naftalena | Gula | |
| Air | |||
| Alkohol | |||
| Benzena |
Jika kita lihat senyawa kovalen: gula dan naftalena – sifat kelarutan mereka berbeda. Hal ini dikarenakan gula merupakan kovalen polar sedangkan naftalena adalah kovalen nonpolar. Air dan alkohol merupakan senyawa polar maka bisa melarutkan gula yang juga polar. Benzena adalah senyawa nonpolar sehingga bisa melarutkan naftalena yang nonpolar.
Pada umumnya, senyawa kovalen polar larut dalam pelarut polar, senyawa kovalen nonpolar larut dalam pelarut nonpolar.