Kimia / Kelas X / Hidrokarbon
Sejauh ini, kita sudah mengetahui atom karbon memiliki nomor atom 6 dengan konfigurasi 2 4. Atom karbon memiliki 4 elektron valensi sehingga dapat membentuk ikatan kovalen.
Karakteristik atom karbon
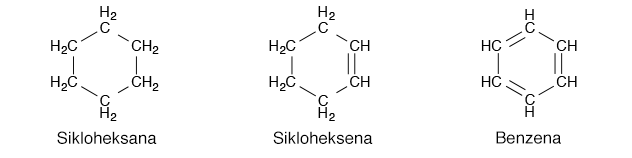
Atom karbon memiliki 4 elektron valensi dengan rumus Lewis seperti diagram di bawah ini. Keempat elektron valensi ini semuanya bisa digunakan untuk membentuk ikatan kovalen. Ikatan kovalen yang paling sederhana adalah saat berikatan dengan 4 atom hidrogen membentuk metana CH4.
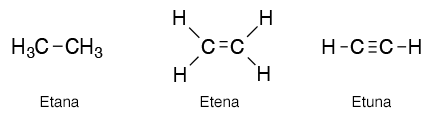
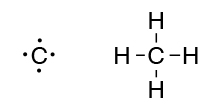 Selain berikatan dengan hidrogen, atom karbon ini juga bisa berikatan dengan atom karbon lainnya, baik dengan ikatan kovalen tunggal ataupun rangkap. Bentuk-bentuk ikatan ini bisa kalian lihat di tata nama senyawa organik.
Selain berikatan dengan hidrogen, atom karbon ini juga bisa berikatan dengan atom karbon lainnya, baik dengan ikatan kovalen tunggal ataupun rangkap. Bentuk-bentuk ikatan ini bisa kalian lihat di tata nama senyawa organik.
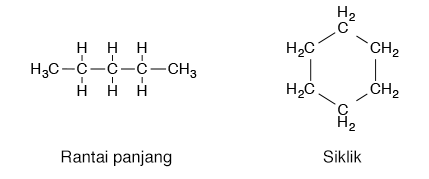
 Kecenderungan atom karbon untuk berikatan dengan atom karbon lainnya memungkinkan senyawa karbon terbentuk dengan berbagai macam struktur. Karbon bisa membentuk rantai panjang atau siklik.
Kecenderungan atom karbon untuk berikatan dengan atom karbon lainnya memungkinkan senyawa karbon terbentuk dengan berbagai macam struktur. Karbon bisa membentuk rantai panjang atau siklik.
Atom karbon primer, sekunder, tersier, dan kuartener
Berdasarkan ikatan karbon dengan atom lainnya, karbon dapat digolongan menjadi atom karbon primer, sekunder, tersier, dan kuartener.
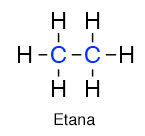
Atom karbon primer dilambangkan dengan seperti 1o adalah atom karbon yang mengikat satu atom karbon tetangga. Contohnya dalam molekul etana CH3 berikatan dengan CH3 juga. Kedua karbon ini merupakan karbon primer karena hanya mengikat satu karbon.
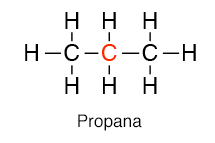
 Atom karbon sekunder dilambangkan dengan seperti ini 2o adalah atom karbon yang mengikat dua atom karbon tetangga. Contohnya pada molekul propana CH3-CH2-CH3. atom karbon pada CH2 yang berada di tengah merupakan atom sekunder karena mengikat 2 atom karbon yang lain.
Atom karbon sekunder dilambangkan dengan seperti ini 2o adalah atom karbon yang mengikat dua atom karbon tetangga. Contohnya pada molekul propana CH3-CH2-CH3. atom karbon pada CH2 yang berada di tengah merupakan atom sekunder karena mengikat 2 atom karbon yang lain.
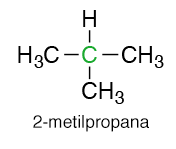
 Atom karbon tersier dengan lambang 3o adalah atom karbon yang mengikat tiga atom karbon tetangga. Contohnya pada molekul 2-metilpropana atau dikenal sebagai isobutana. Karbon CH yang berada di tengah adalah karbon tersier karena mengikat 3 karbon.
Atom karbon tersier dengan lambang 3o adalah atom karbon yang mengikat tiga atom karbon tetangga. Contohnya pada molekul 2-metilpropana atau dikenal sebagai isobutana. Karbon CH yang berada di tengah adalah karbon tersier karena mengikat 3 karbon.
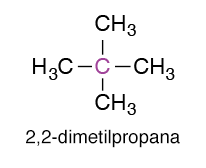
 Atom karbon kuartener dilambangkan dengan 4o adalah atom karbon yang mengikat empat karbon yang lainnya. Jadi semua elektron valensinya dipakai untuk mengikat karbon tetangganya. Contohnya pada molekul 2,2-dimetilpropana. Atom C yang di tengah ini adalah karbon kuartener karena mengikat empat karbon.
Atom karbon kuartener dilambangkan dengan 4o adalah atom karbon yang mengikat empat karbon yang lainnya. Jadi semua elektron valensinya dipakai untuk mengikat karbon tetangganya. Contohnya pada molekul 2,2-dimetilpropana. Atom C yang di tengah ini adalah karbon kuartener karena mengikat empat karbon.
Karakteristik atom karbon
Atom karbon memiliki 4 elektron valensi dengan rumus Lewis seperti diagram di bawah ini. Keempat elektron valensi ini semuanya bisa digunakan untuk membentuk ikatan kovalen. Ikatan kovalen yang paling sederhana adalah saat berikatan dengan 4 atom hidrogen membentuk metana CH4.
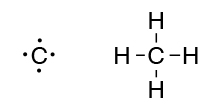


Atom karbon primer, sekunder, tersier, dan kuartener
Berdasarkan ikatan karbon dengan atom lainnya, karbon dapat digolongan menjadi atom karbon primer, sekunder, tersier, dan kuartener.
Atom karbon primer dilambangkan dengan seperti 1o adalah atom karbon yang mengikat satu atom karbon tetangga. Contohnya dalam molekul etana CH3 berikatan dengan CH3 juga. Kedua karbon ini merupakan karbon primer karena hanya mengikat satu karbon.




Identifikasi karbon dan hidrogen
Keberadaan unsur karbon dan hidrogen dalam bentuk senyawa hidrokarbon dapat diidentifikasi dengan percobaan sederhana. Salah satu contohnya adalah dengan menggunakan lilin yang merupakan senyawa hidrokarbon dengan rumus C20H42. Lilin ini dibakar, yang merupakan reaksi dengan O2. Hasil pembakaran ini dilarutkan ke dalam larutan kalsium hidroksida Ca(OH)2. Kenapa cara ini bisa mengidentifikasi adanya hidrokarbon?
Pertama, kita lihat reaksi yang terjadi saat lilin ini bereaksi dengan oksigen. Reaksi hidrokarbon dan oksigen selalu menghasilkan gas karbon dioksida dan uap air.
Karbon dioksida iniliah yang kita alirkan dari pembakaran ini ke larutan kalsium hidroksida. CO2 ini memiliki titik embun yang sangat rendah sehingga tetap berupa gas saat dialirkan dan bereaksi dengan kalsium hidroksida tersebut. Reaksi ini memiliki persamaan:
Kalsium karbonat inilah yang membuat larutan jenuh, kejenuhan larutan menunjukkan adanya senyawa hidrokarbon.
Klarifikasi hidrokarbon
Pada dasarnya, senyawa karbon digolongkan menjadi hidrokarbon dan turunan hidrokarbon. Turunan hidrokarbon adalah senyawa karbon yang mengandung atom-atom selain karbon dan hidrogen, seperti alkohol, aldehida, dan protein. Dari cara berikatan antara karbon-karbon, senyawa hidrokarbon bisa dikelompokkan menjadi 2:
Senyawa hidrokarbon alifatik
Senyawa hidrokarbon alifatik adalah senyawa hidrokarbon yang membentuk rantai dengan ujung terbuka, baik berupa rantai lurus ataupun bercabang. Senyawa alifatik sendiri masih bisa digolongkan menjadi 2 lagi:
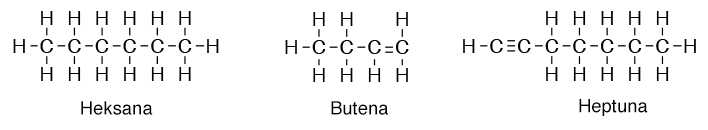
• Senyawa hidrokarbon alifatik jenuh: senyawa hidrokarbon yang hanya memiliki ikatan tunggal saja. Contohnya adalah senyawa jenis alkana seperti heksana dan propana.
• Senyawa hidrokarbon tidak jenuh: senyawa karbon yang memiliki minimal satu ikatan rangkap, bisa berupa ikatan rangkap dua atau tiga. Contohnya adalah senyawa jenis alkena dan alkuna seperti butena dan heptuna.
Senywa hidrokarbon siklik
Senyawa hidrokarbon siklik adalah senyawa hidrokarbon yang berbentuk rantai tertutup. Senyawa siklik dibagi menjadi 2 lagi:
• Senyawa hidrokarbon alisiklik: senyawa alifatik yang rantainya tertutup. Contohnya sikloheksana dan sikloheksena.
• Senyawa hidrokarbon aromatik: senyawa jenis benzena (memiliki elektron yang terdelokasi) dan turunannya. Contohnya benzena, naftalena, toluena, dan nitrobenzena.
Keberadaan unsur karbon dan hidrogen dalam bentuk senyawa hidrokarbon dapat diidentifikasi dengan percobaan sederhana. Salah satu contohnya adalah dengan menggunakan lilin yang merupakan senyawa hidrokarbon dengan rumus C20H42. Lilin ini dibakar, yang merupakan reaksi dengan O2. Hasil pembakaran ini dilarutkan ke dalam larutan kalsium hidroksida Ca(OH)2. Kenapa cara ini bisa mengidentifikasi adanya hidrokarbon?
Pertama, kita lihat reaksi yang terjadi saat lilin ini bereaksi dengan oksigen. Reaksi hidrokarbon dan oksigen selalu menghasilkan gas karbon dioksida dan uap air.
2C20H24(s) + 61O2(g) ➝ 40CO2(g) + 42H2O(g)
CO2(g) + Ca(OH)2(aq) ➝ CaCO3(s) + H2O(l)
Klarifikasi hidrokarbon
Pada dasarnya, senyawa karbon digolongkan menjadi hidrokarbon dan turunan hidrokarbon. Turunan hidrokarbon adalah senyawa karbon yang mengandung atom-atom selain karbon dan hidrogen, seperti alkohol, aldehida, dan protein. Dari cara berikatan antara karbon-karbon, senyawa hidrokarbon bisa dikelompokkan menjadi 2:
Senyawa hidrokarbon alifatik
Senyawa hidrokarbon alifatik adalah senyawa hidrokarbon yang membentuk rantai dengan ujung terbuka, baik berupa rantai lurus ataupun bercabang. Senyawa alifatik sendiri masih bisa digolongkan menjadi 2 lagi:
• Senyawa hidrokarbon alifatik jenuh: senyawa hidrokarbon yang hanya memiliki ikatan tunggal saja. Contohnya adalah senyawa jenis alkana seperti heksana dan propana.
• Senyawa hidrokarbon tidak jenuh: senyawa karbon yang memiliki minimal satu ikatan rangkap, bisa berupa ikatan rangkap dua atau tiga. Contohnya adalah senyawa jenis alkena dan alkuna seperti butena dan heptuna.

Senywa hidrokarbon siklik
Senyawa hidrokarbon siklik adalah senyawa hidrokarbon yang berbentuk rantai tertutup. Senyawa siklik dibagi menjadi 2 lagi:
• Senyawa hidrokarbon alisiklik: senyawa alifatik yang rantainya tertutup. Contohnya sikloheksana dan sikloheksena.
• Senyawa hidrokarbon aromatik: senyawa jenis benzena (memiliki elektron yang terdelokasi) dan turunannya. Contohnya benzena, naftalena, toluena, dan nitrobenzena.

Berdasarkan jumlah ikatan antara atom karbon, senyawa alifatik digolongkan menjadi dua: jenuh dan tidak jenuh. Karbon digolongkan alifatik jenuh ketika dapat mengikat hidrogen secara maksimal yang berarti dengan kata lain tidak memiliki ikatan rangkap sama sekali. Senyawa yang tergolong alifatik jenuh adalah alkana dan sikloalkana.
Struktur dan sifat alkana
Senyawa alkana yang paling sedeharna adalah metana CH4, 1 atom karbon mengikat 4 atom hidrogen. Struktur molekul alkana yang lebih panjang contohnya adalah etana, propana, butana, dan lainnya. Struktur alkana pada umumnya dituliskan dengan rumus struktur yang dimampatkan.
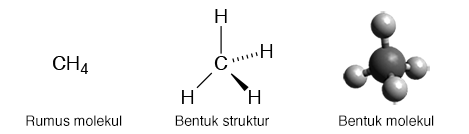 Berdasarkan contoh di atas, dari metana ke butana selalu terdapat selisih gugus –CH2-. Etana memiliki satu gugus –CH2- lebih dari metana. Propana memiliki satu gugus –CH2- lebih dari etana dan seterusnya. Di dalam suatu deret senyawa yang memiliki selisih jumlah gugus –CH2- secara berurutan disebut dengan deret homolog. Senyawa-senyawa di dalam satu deret homolog memiliki sifat kimia yang mirip, tetapi sifat fisikanya berubah seiring dengan kenaikan massa molekul seperti tabel di bawah ini:
Berdasarkan contoh di atas, dari metana ke butana selalu terdapat selisih gugus –CH2-. Etana memiliki satu gugus –CH2- lebih dari metana. Propana memiliki satu gugus –CH2- lebih dari etana dan seterusnya. Di dalam suatu deret senyawa yang memiliki selisih jumlah gugus –CH2- secara berurutan disebut dengan deret homolog. Senyawa-senyawa di dalam satu deret homolog memiliki sifat kimia yang mirip, tetapi sifat fisikanya berubah seiring dengan kenaikan massa molekul seperti tabel di bawah ini:
Dengan bertambahnya massa molekul, wujud zat juga berubah. Empat deret pertama alkana berbentuk gas, lalu deret berikutnya berupa cair. Pada alkana yang lebih panjang berwujud padat, contohnya lilin (C20H24). Semua alkana dapat bereaksi dengan oksigen membentuk karbon dioksida dan uap air yang memiliki persamaan:
Di dalam deret homolog terdapat selisih sebanyak –CH2-. Jika tambahannya sebanyak n gugus maka terdapat selisih (–CH2-)n atau –CnH2n-. Maka rumus umum alkana CnH2n+2.
Tata nama alkana
Ada lima pokok aturan IUPAC untuk penamaan alkana yaitu:
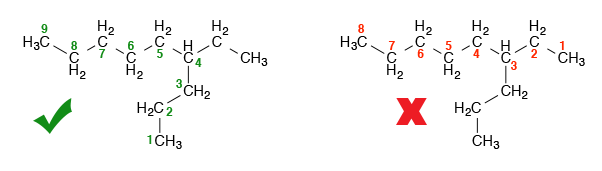
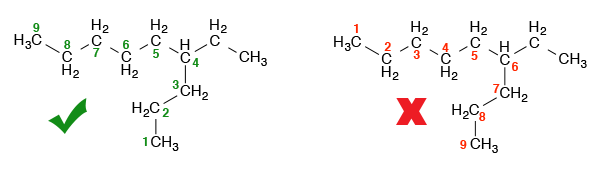
1. Pada alkana yang memiliki rantai bercabang, nama dasar alkana ditentukan oleh rantai yang memiliki karbon paling banyak. Rantai terpanjang ini disebut dengan rantai induk. Contohnya pada rantai di bawah ini, rantai induk yang benar adalah yang terdiri dari 9 karbon.
 2. Cabang dari rantai induk disebut dengan gugus alkil. Nama gugus alkil adalah berdasarkan nama alkana semula tetapi akhiran –ana diganti menjadi –il. Contohnya seperti tabel di bawah ini:
2. Cabang dari rantai induk disebut dengan gugus alkil. Nama gugus alkil adalah berdasarkan nama alkana semula tetapi akhiran –ana diganti menjadi –il. Contohnya seperti tabel di bawah ini:
3. Gugus alkil yang terikat pada rantai iduk diberi nomor dengan urutan yang terkecil. Jadi untuk rantai seperti contoh yang sebelumnya, penomoran yang benar adalah yang berwarna hijau. Jadi nama senyawa tersebut adalah 4-etilnonana bukan 6-etilnonana.
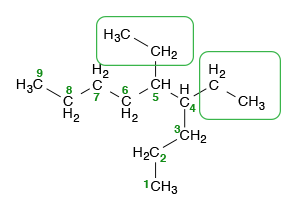
 4. Jika ada gugus alkil yang sama pada karbon yang berbeda di rantai induk, nama gugus ditambah dengan kata depan di- untuk dua gugus, tri- untuk tiga gugus, dan tetra- untuk empat gugus. Contohnya seperti pada senyawa di bawah ini disebut dengan 4,5-dietilnonana.
4. Jika ada gugus alkil yang sama pada karbon yang berbeda di rantai induk, nama gugus ditambah dengan kata depan di- untuk dua gugus, tri- untuk tiga gugus, dan tetra- untuk empat gugus. Contohnya seperti pada senyawa di bawah ini disebut dengan 4,5-dietilnonana.
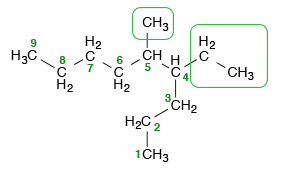
 5. Jika terdapat dua atau lebih cabang alkil yang berbeda gugus, maka penulisannya berdasarkan alfabetis. Contohnya pada molekul ini ditulis 4-etil-5-metilnonana bukan 5-metil-4-etilnonana.
5. Jika terdapat dua atau lebih cabang alkil yang berbeda gugus, maka penulisannya berdasarkan alfabetis. Contohnya pada molekul ini ditulis 4-etil-5-metilnonana bukan 5-metil-4-etilnonana.
Isomer alkana
Struktur alkana bisa berbentuk rantai lurus ataupun bercabang. Oleh karena itu, satu rumus molekul bisa memiliki rumus struktur yang berbeda. Contohnya pada C4H10 bisa memiliki rumus struktur seperti berikut:
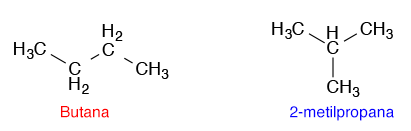 Pada rantai lurus tak bercabang disebut dengan butana. Senyawa yang bercabang ini disebut dengan 2-metilpropana atau isobutana. Kedua senyawa ini memiliki sifat fisika yang berbeda, titik didih dan titik lelehnya berbeda. Senyawa butana memiliki titik leleh sekitar -135oC dan titik didih sekitar -0,5oC. Isobutana memiliki titik leleh pada -145oC dan titik didih pada -10oC. Senyawa yang memiliki rumus molekul sama tetapi beda struktur disebut dengan isomer. Oleh karena perbedaan molekul ini terletak pada strukturnya maka disebut dengan isomer struktur.
Pada rantai lurus tak bercabang disebut dengan butana. Senyawa yang bercabang ini disebut dengan 2-metilpropana atau isobutana. Kedua senyawa ini memiliki sifat fisika yang berbeda, titik didih dan titik lelehnya berbeda. Senyawa butana memiliki titik leleh sekitar -135oC dan titik didih sekitar -0,5oC. Isobutana memiliki titik leleh pada -145oC dan titik didih pada -10oC. Senyawa yang memiliki rumus molekul sama tetapi beda struktur disebut dengan isomer. Oleh karena perbedaan molekul ini terletak pada strukturnya maka disebut dengan isomer struktur.
Semakin banyak jumlah karbonnya, semakin banyak isomer yang dimiliki. Pentana C5H12 memiliki 3 isomer, heksana C6H14 memiliki 5 isomer, dekana C10H22 memiliki 75 isomer.
Pada senyawa pentana, titik didih dan titik lelehnya berkurang dengan urutan: n-pentana > isopentana > neopentana. Intinya, titik didih dan titik leleh semakin tinggi dengan semakin panjang rantai induknya.
Struktur dan sifat alkana
Senyawa alkana yang paling sedeharna adalah metana CH4, 1 atom karbon mengikat 4 atom hidrogen. Struktur molekul alkana yang lebih panjang contohnya adalah etana, propana, butana, dan lainnya. Struktur alkana pada umumnya dituliskan dengan rumus struktur yang dimampatkan.

| Nama Senyawa | Rumus Molekul | Massa Molekul | Wujud Molekul | Titik Leleh (oC) | Titik Didih (oC) |
| Metana | CH4 | 16 | Gas | -182,5 | -164,0 |
| Etana | C2H6 | 30 | Gas | -183,3 | -88,6 |
| Propana | C3H8 | 44 | Gas | -189,7 | -42,1 |
| Butana | C4H10 | 58 | Gas | -138,4 | 0,5 |
| Pentana | C5H12 | 72 | Cair | -139,7 | 36,1 |
| Heksana | C6H14 | 86 | Cair | -95,0 | 68,9 |
| Heptana | C7H16 | 100 | Cair | -90,6 | 98,4 |
| Oktana | C8H18 | 114 | Cair | -56,8 | 124,7 |
| Nonana | C9H20 | 128 | Cair | -51,0 | 150,8 |
| Dekana | C10H22 | 142 | Cair | -29,7 | 174,1 |
Dengan bertambahnya massa molekul, wujud zat juga berubah. Empat deret pertama alkana berbentuk gas, lalu deret berikutnya berupa cair. Pada alkana yang lebih panjang berwujud padat, contohnya lilin (C20H24). Semua alkana dapat bereaksi dengan oksigen membentuk karbon dioksida dan uap air yang memiliki persamaan:
CnH2n+2 + O2(g) ➝ nCO2(g) + (n+1)H2O(g)
Tata nama alkana
Ada lima pokok aturan IUPAC untuk penamaan alkana yaitu:
1. Pada alkana yang memiliki rantai bercabang, nama dasar alkana ditentukan oleh rantai yang memiliki karbon paling banyak. Rantai terpanjang ini disebut dengan rantai induk. Contohnya pada rantai di bawah ini, rantai induk yang benar adalah yang terdiri dari 9 karbon.

| Gugus alkil | Tata Nama |
| -CH3 | metil |
| -C2H5 | etil |
| -C3H7 | propil |
| -C4H9 | butil |
| -C5H11 | pentil |
| Gugus alkil | Tata Nama |
| -C6H13 | heksil |
| -C7H15 | heptil |
| -C8H17 | oktil |
| -C9H19 | nonil |
| -C10H21 | dekil |



Isomer alkana
Struktur alkana bisa berbentuk rantai lurus ataupun bercabang. Oleh karena itu, satu rumus molekul bisa memiliki rumus struktur yang berbeda. Contohnya pada C4H10 bisa memiliki rumus struktur seperti berikut:
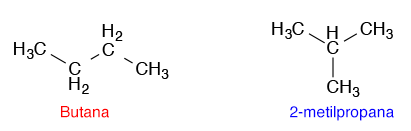
Semakin banyak jumlah karbonnya, semakin banyak isomer yang dimiliki. Pentana C5H12 memiliki 3 isomer, heksana C6H14 memiliki 5 isomer, dekana C10H22 memiliki 75 isomer.
Pada senyawa pentana, titik didih dan titik lelehnya berkurang dengan urutan: n-pentana > isopentana > neopentana. Intinya, titik didih dan titik leleh semakin tinggi dengan semakin panjang rantai induknya.
Hidrokarbon tidak jenuh adalah hidrokarbon yang memiliki satu atau lebih ikatan rangkap. Ikatan rangkap tersebut dapat berupa ikatan rangkap dua (alkena) ataupun ikatan rangkap tiga (alkuna).
Struktur dan sifat alkena
Alkena yang paling sederhana adalah etena yang terdiri dari 2 karbon dengan struktur seperti ini:
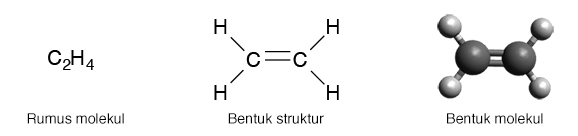 Di dalam alkena bisa terdapat satu atau lebih ikatan rangkap dua. Deret homolog alkena dengan satu ikatan rangkap adalah etena, propena, butena, dan seterusnya.
Di dalam alkena bisa terdapat satu atau lebih ikatan rangkap dua. Deret homolog alkena dengan satu ikatan rangkap adalah etena, propena, butena, dan seterusnya.
Sama seperti alkana, alkena juga memiliki selisih –CH2- antar deret homolog (kecuali dari etena ke propena). Alkena memiliki rumus CnH2n. Secara umum, titik didih dan titik leleh alkena memiliki sifat yang mirip dengan alkana. Titik didih dan titik leleh semakin meningkat dengan semakin panjangnya rantai induk.
Tata nama dan isomer alkena
Tata nama alkena pada umumnya sama seperti alkana hanya saja akhirannya berubah menjadi –ena. Beberapa aturan khusus alkena yaitu penomoran atom karbon dimulai dari ujung rantai yang terdekat dengan ikatan rangkap dua nya. Contohnya:
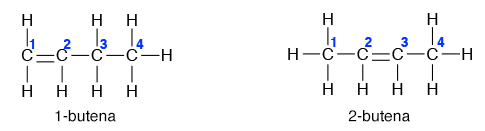 Jika di dalam molekul terdapat dua atau lebih ikatan rangkap maka namanya ditambahkan dengan di-, tri-, dan seterusnya. Contohnya:
Jika di dalam molekul terdapat dua atau lebih ikatan rangkap maka namanya ditambahkan dengan di-, tri-, dan seterusnya. Contohnya:
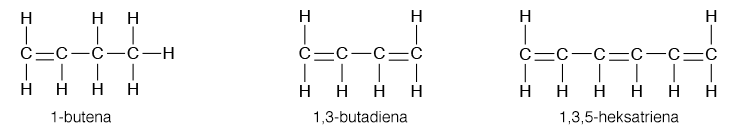 Sama seperti pada alkana, alkena memiliki isomer struktur.Rumus molekul C4H8 bisa memiliki tiga macam isomer:
Sama seperti pada alkana, alkena memiliki isomer struktur.Rumus molekul C4H8 bisa memiliki tiga macam isomer:
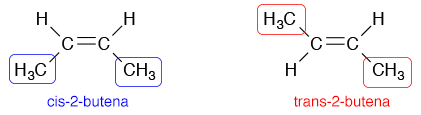
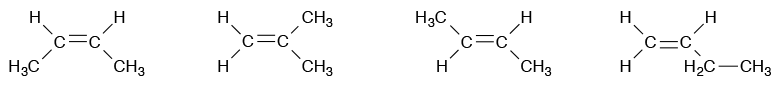 Selain itu, karena adanya ikatan rangkap dua yang berupa rigid dan tidak bisa diputar, alkena bisa membentuk isomer geometri. Contohnya pada 2-butena, terdapat 2 isomer geometri yaitu cis-2-butena (Z-butena) dan trans-2-butena (E-butena). Perbedaan cis dan trans adalah letak di mana molekul terbesar setelah ikatan rangkap itu. Jika kedua molekul yang besar berada pada sisi yang sama, maka disebut cis (Z). Jika berada pada sisi yang berbeda maka disebut trans (E).
Selain itu, karena adanya ikatan rangkap dua yang berupa rigid dan tidak bisa diputar, alkena bisa membentuk isomer geometri. Contohnya pada 2-butena, terdapat 2 isomer geometri yaitu cis-2-butena (Z-butena) dan trans-2-butena (E-butena). Perbedaan cis dan trans adalah letak di mana molekul terbesar setelah ikatan rangkap itu. Jika kedua molekul yang besar berada pada sisi yang sama, maka disebut cis (Z). Jika berada pada sisi yang berbeda maka disebut trans (E).
 Isomer lain yang ada pada alkena adalah isomer posisi. Isomer ini adalah perbedaan letak ikatan rangkap dua berada. Contohnya: 1-butena dan 2-butena.
Isomer lain yang ada pada alkena adalah isomer posisi. Isomer ini adalah perbedaan letak ikatan rangkap dua berada. Contohnya: 1-butena dan 2-butena.
Strukture dan tata nama alkuna
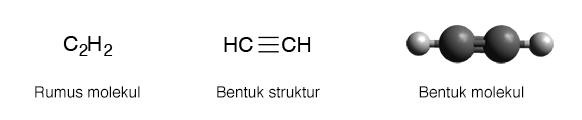
Alkuna adalah hidrokarbon tidak jenuh yang memiliki minimal satu ikatan rangkap tiga. Struktur alkuna yang paling sederhana adalah etuna C2H2. Ikatan rangkap tiga ini sangatlah rigid sehingga struktur molekulnya berbentuk linear.
 Etuna dapat dibuat dengan mereaksikan CaC2 dan air.
Etuna dapat dibuat dengan mereaksikan CaC2 dan air.
Alkuna memiliki rumus CnH2n-2.Tata nama alkuna tetap mirip dengan alkana dan alkena, hanya saja akhirannya diganti dengan –una. Empat deret homolog pertama alkuna adalah etuna, propuna, 1-butuna, dan 1-pentuna.
Alkuna memiliki isomer struktur seperti pada alkana dan alkena. Alkuna tidak memiliki isomer geometri karena strukturnya yang rigid dan berbentuk linear. Alkuna memiliki isomer posisi seperti pada alkena.
Struktur dan sifat alkena
Alkena yang paling sederhana adalah etena yang terdiri dari 2 karbon dengan struktur seperti ini:

Sama seperti alkana, alkena juga memiliki selisih –CH2- antar deret homolog (kecuali dari etena ke propena). Alkena memiliki rumus CnH2n. Secara umum, titik didih dan titik leleh alkena memiliki sifat yang mirip dengan alkana. Titik didih dan titik leleh semakin meningkat dengan semakin panjangnya rantai induk.
Tata nama dan isomer alkena
Tata nama alkena pada umumnya sama seperti alkana hanya saja akhirannya berubah menjadi –ena. Beberapa aturan khusus alkena yaitu penomoran atom karbon dimulai dari ujung rantai yang terdekat dengan ikatan rangkap dua nya. Contohnya:
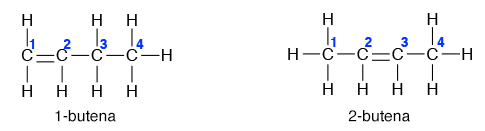

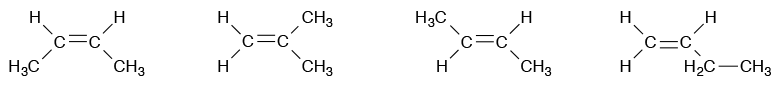

Strukture dan tata nama alkuna
Alkuna adalah hidrokarbon tidak jenuh yang memiliki minimal satu ikatan rangkap tiga. Struktur alkuna yang paling sederhana adalah etuna C2H2. Ikatan rangkap tiga ini sangatlah rigid sehingga struktur molekulnya berbentuk linear.

CaC2(s) + 2H2O(l) ➝ C2H2(g) + Ca(OH)2(s)
Alkuna memiliki isomer struktur seperti pada alkana dan alkena. Alkuna tidak memiliki isomer geometri karena strukturnya yang rigid dan berbentuk linear. Alkuna memiliki isomer posisi seperti pada alkena.